中興大學化學系李進發終身特聘教授兼系主任,與加州大學洛杉磯分校(UCLA)前奈米中心(CNSI)主任Paul S. Weiss教授、分子藥理所曾憲榮教授組成的前瞻研究團隊,利用奈米技術大幅改善CRISPR / Cas9基因編輯系統對於標靶細胞的遞送效率。該技術提供遺傳疾病患者臨床治療的解決方案,成果於6月發表在國際權威期刊《Small》。
去年諾貝爾化學獎得主即是以發現CRISPR/Cas9基因編輯系統獲得肯定,主要靈感來自細菌中既存的基因組編輯系統,當細菌被病毒感染時,會將病毒DNA編進自己的基因組中,日後若面對相同病毒,即可辨識並切割掉有害病毒,又稱「基因剪刀」,可精準地改變動物、植物和微生物的DNA。
李進發表示,迅速有效的CRISPR / Cas9基因編輯技術已廣泛應用於基礎研究、生技產品開發及醫學研究,然而脱靶(off target)效應及遞送工具的選擇是此技術急需突破的主要關鍵。尤其在醫學基因疾病治療上,脱靶效應可能產生的副作用將影響CRISPR技術在臨床應用的發展,因此發展高效遞送策略的載體是該領域的重要前沿研究。
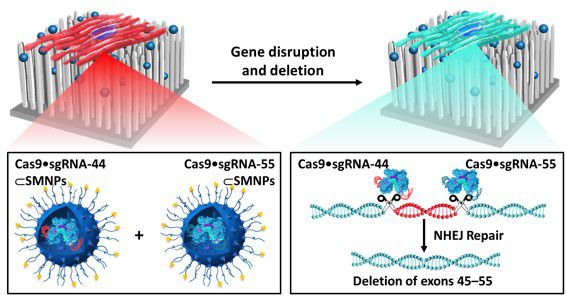
此研究透過分子辨識技術,促進超分子奈米顆粒聚集於奈米線,確保CRISPR / Cas9系統進行基因編輯的效率,同時也降低脫靶效應。此一研究成果不僅在為治療基因遺傳疾病提供革命性的新思路及新希望外,由於在基礎醫學、藥理學、生物學、以及農業科技等相關領域上均能被廣泛應用的潛力,備受國際重視。
==========================================================
興大跨國團隊提升CRISPR / Cas9基因編輯系統遞送效率 登頂尖期刊《Small》
稿源:2021-06-11/中央社
中興大學化學系李進發終身特聘教授兼系主任,與加州大學洛杉磯分校(UCLA)前奈米中心(CNSI)主任Paul S. Weiss教授、分子藥理所曾憲榮教授組成的前瞻研究團隊,利用奈米技術大幅改善CRISPR / Cas9基因編輯系統對於標靶細胞的遞送效率。該技術提供遺傳疾病患者臨床治療的解決方案,成果於6月發表在國際權威期刊《Small》。
去年諾貝爾化學獎得主即是以發現CRISPR/Cas9基因編輯系統獲得肯定,主要靈感來自細菌中既存的基因組編輯系統,當細菌被病毒感染時,會將病毒DNA編進自己的基因組中,日後若面對相同病毒,即可辨識並切割掉有害病毒,又稱「基因剪刀」,可精準地改變動物、植物和微生物的DNA。
李進發表示,迅速有效的CRISPR / Cas9基因編輯技術已廣泛應用於基礎研究、生技產品開發及醫學研究,然而脱靶(off target)效應及遞送工具的選擇是此技術急需突破的主要關鍵。尤其在醫學基因疾病治療上,脱靶效應可能產生的副作用將影響CRISPR技術在臨床應用的發展,因此發展高效遞送策略的載體是該領域的重要前沿研究。
此研究透過分子辨識技術,促進超分子奈米顆粒聚集於奈米線,確保CRISPR / Cas9系統進行基因編輯的效率,同時也降低脫靶效應。此一研究成果不僅在為治療基因遺傳疾病提供革命性的新思路及新希望外,由於在基礎醫學、藥理學、生物學、以及農業科技等相關領域上均能被廣泛應用的潛力,備受國際重視。
訊息來源:國立中興大學
本文含多媒體檔 (Multimedia files included): http://www.cna.com.tw/postwrite/Detail/294564.aspx

圖說:左而右: 中興大學校長薛富盛教授、加州大學洛杉磯分校(UCLA)分子藥理所曾憲榮教授、中興大學化學系李進發教授
照片圖說:超分子奈米顆粒介導CRISPR / Cas9系統的傳輸